Fala Gás Nobre, hoje vamos fazer um resumão sobre os efeitos indutivos, que influenciam na acidez e na coloração de moléculas, geralmente orgânicas.
O efeito indutivo é um efeito que pode ser observado experimentalmente e trata-se da transmissão de carga eletrônica, na forma de elétrons, através das ligações químicas de uma molécula por indução eletrostática.
É importante ressaltar que este efeito é observado em moléculas que possuem ligações covalentes, ou seja, moléculas que realizam ligações através do compartilhamento de elétrons.
Leia mais em:
Ligações Covalentes no nosso cotidiano: Parte I
Ligações Covalente no nosso cotidiano: Parte II
A ligação covalente simples é uma ligação σ (sigma). A nuvem eletrônica nesta ligação, quando ocorre entre dois átomos diferentes, não é uniforme, isto é, é levemente deslocada em direção ao átomo mais eletronegativo. Essa não uniformidade causa um permanente estado de polarização da ligação, formando uma leve densidade de cargas negativas (δ–) no átomo mais eletronegativo e uma leve densidade de cargas positivas (δ+) no outro.
Lembrando que eletronegatividade é a tendência a receber elétrons, quanto mais eletronegativo um elemento, maior será esta tendência.
Se este átomo eletronegativo, por exemplo, está ligado em uma cadeia carbônica, sua atração faz com que o efeito de densidade de cargas positivas seja observado ao longo da cadeia. Chamamos isso de efeito indutivo negativo, quando a tendência de afastar o elétron se espalha pela cadeia. Este efeito torna-se mais fraco ao longo da cadeia, quanto mais distante do átomo eletronegativo, mais fraco o efeito.
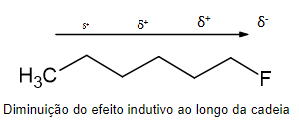
Isso significa que moléculas com presença de átomos eletronegativos vão manter-se estáveis mesmo se perderem um átomo de hidrogênio e apresentarem carga negativa.
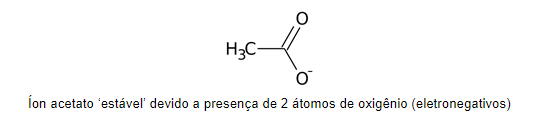
No entanto, alguns grupos funcionais, como os grupos alquilas, que são constituídos por hidrocarbonetos, isto é, carbonos e hidrogênios, apresentam o efeito contrário, o efeito indutivo positivo. Isso significa que estas moléculas vão se manter estáveis mesmo na presença de uma carga negativa em sua cadeia.
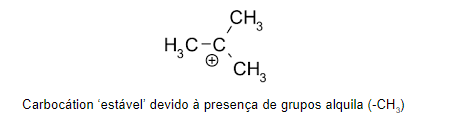
Carbonos com carga positiva são chamados de carbocátions e são muito utilizados em inúmeros processos de síntese de compostos orgânicos.
O efeito indutivo vai ser mais ou menos intenso de acordo com o grupo funcional presente, se ele é retirador ou liberador de elétrons e pelo tamanho da cadeia. Por isso é importante saber reconhecer o tipo de função presente na molécula.
Leia mais em:
Reconhecimento das Funções Orgânicas
Funções Oxigenadas
Funções Nitrogenadas
Este efeito também pode ser causado em moléculas vizinhas, um dipolo permanente na molécula pode gerar um momento dipolo induzido em outra molécula, ou interagir com um dipolo permanente de outra molécula.
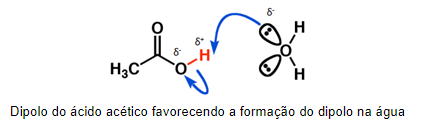
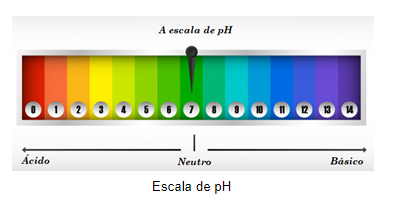
Uma das propriedades afetadas pelo efeito indutivo é o pH. O pH, ou potencial hidrogeniônico, é uma escala de medida que determina a acidez e basicidade de compostos e soluções químicas. Essa escala varia de 0 à 14, sendo 7 o valor de uma pH neutro, tipo o da água, abaixo de 7 ácido, isto é, quanto mais próximo de 0, mas ácido será o composto e 7 neutro, logo, quanto mais próximo de 14, mais básico.
Leia mais em:
pH e pOH
pH: O que você precisa saber?
A presença de grupos funcionais que contém átomos retiradores de elétrons (F, Cl, Br, I, O, N), ou seja, eletronegativos, ocasiona no aumento da acidez de compostos orgânicos. O efeito retirador de elétrons estabiliza a carga negativa formada na molécula ao liberar H+, fazendo com que a molécula libere mais facilmente seu hidrogênio ácido, aumentando assim sua acidez se comparada a outras moléculas semelhantes.
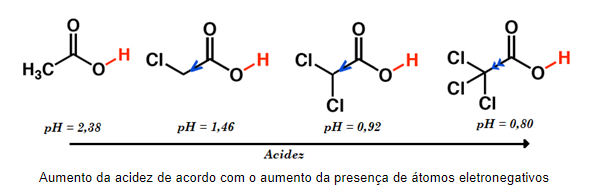
O efeito indutivo causado por esses átomos é tão grande que podemos observar que um ácido orgânico, como o ácido acético (figura acima), considerado fraco, passa a ter um pH semelhante ao de ácidos inorgânicos fortes, como ácido clorídrico (HCl) e sulfúrico (H2SO4).
Leia mais em:
Teorias Ácido-Base: Exercícios Resolvidos
Ácidos e Bases no ENEM
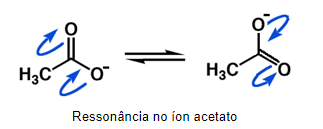
Outro efeito indutivo é o chamado de “efeito mesomérico”, que é também conhecido como “efeito de ressonância”, que está diretamente relacionado a moléculas que contenham pelo menos 1 ligação dupla (ligação do tipo π).
Este efeito é bem semelhante ao que estamos falando até agora, no entanto, difere pelo fluxo de elétrons presentes nas ligações duplas. Esses pares de elétrons podem entrar em ressonância para melhor estabilizar uma densidade de cargas presentes na molécula.
Esse efeito de ressonância pode ser observado também em moléculas que possuem mais de uma ligação dupla. Quantos estas ligações estão conjugadas, por exemplo, uma ligação simples e uma dupla intercaladas na molécula, esse efeito é forte e espalha-se por toda região onde se encontram estas duplas ligações.
Esse efeito de ressonância nas duplas conjugadas pode ser observado no anel benzênico, que é representado com um círculo no seu interior, que representa exatamente esse fluxo do par de elétrons entre um ligação dupla e outra.
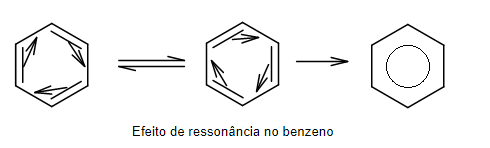
Algo digno de nota é que este efeito de fluxo de elétrons é o que atribui coloração aos compostos orgânicas. Os compostos orgânicos mais comuns geralmente são gases e líquidos incolores e sólidos brancos, como por exemplo, álcool, acetona, vinagre, vitamina C, amido, açúcar, entre outros.
No entanto, os compostos orgânicos que apresentam ressonância possuem cor, podendo ser analisados por técnicas espectrofotométricas, que determinam a concentração de uma solução de acordo com a quantidade de luz absorvida.
Leia mais em:
Introdução à Espectrofotometria
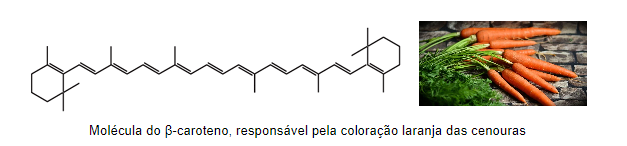
Um exemplo destes compostos com duplas ligações conjugadas é o β-caroteno, molécula responsável pela coloração laranja das cenouras. Devido ao tamanho da sua cadeia e o elevado número de duplas conjugadas em ressonância, esta molécula é um protetor natural contra a radiação UV dos raios solares. No entanto, uma alimentação muita rica em β-caroteno, em casos muito raros, pode resultar na carotenodermia, que é o amarelamento da pele.
Para encerrar, podemos concluir que:
– Efeito indutivo de estabilização de uma carga negativa é maior na presença de um ou mais grupos retiradores de elétrons, isto é, átomos eletronegativos ou grupos funcionais ligados a átomos eletronegativos (F, Cl, Br, I, O, N)
– Efeito indutivo de estabilização de uma carga positiva (carbocátion) é maior na presença de um ou mais grupos alquila (hidrocarbonetos).
– Efeito indutivo interfere na acidez de um composto, tornando-o mais ou menos ácido.
– Efeito de ressonância ocorre devido a presença de pelo menos uma ligação dupla (π).
– Se a molécula possuir mais de uma ligação dupla e estas estiverem intercaladas com ligações simples observamos o que chamamos de ligações duplas conjugadas.
– Quanto maior o número de ligações duplas conjugadas, maior o efeito de ressonância.
– Moléculas orgânicas com duplas ligações conjugadas apresentam coloração.
Certo Gás Nobre? Esse foi um super resumão dos efeitos indutivos, onde falamos das relações de estabilidade de carga, influencia no pH, ressonância e coloração de compostos.
Gás Nobre! Você tem dificuldades para entender conteúdos de Ciências da Natureza? Não fique triste! Eu, professor Paulo Valim, quero te contar um segredinho que os melhores estudantes do Brasil já conhecem, com a minha plataforma Ciência em Ação, você vai conseguir aprender Química, Física e Biologia de forma rápida e efetiva e garantir a sua aprovação ainda em 2020.
Não importa se você tem dificuldades com as matérias ou se essa é a primeira vez que você vai estudar Química, Física ou Biologia. No Ciência em Ação, nossos cursos são completos e aprofundados. Eu e a minha equipe ensinamos todo o conteúdo do começo ao fim de forma didática.
Que foi? Você tem dúvidas de que o que eu estou falando é verdade? Então, saca só, Gás Nobre! Liberei o primeiro módulo completo da minha plataforma Ciência em Ação totalmente grátis pra você experimentar! Curtiu? Clique aqui e aproveite para conhecer a melhor plataforma de Ciências da Natureza da web!
Bora reagir e realizar os seus sonhos?
Me acompanhe nas redes sociais: curta a minha página no Facebook, siga o meu Instagram, se inscreva no canal do Youtube e entre no meu canal do Telegram.