Fala, Gás Nobre!
Neste post, trouxemos alguns exercícios sobre classificação dos elementos na Tabela Periódica. Esse tipo de exercício é bastante importante para ajudar a fixar os conhecimentos relacionados à tabela, números atômicos, configuração eletrônica, e recorrência das propriedades periódicas etc. Eles foram retirados do Enem e de alguns outros vestibulares importantes realizados no país. Então, acompanhe e bons estudos!
Exercícios sobre Classificação dos Elementos na Tabela
1. (Ufam-AM) Na classificação periódica, os elementos Ba (grupo 2), Se (grupo 16) e Cl (grupo 17) são conhecidos, respectivamente, como:
a) alcalino, halogênio e calcogênio
b) alcalino terroso, halogênio e calcogênio
c) alcalino terroso, calcogênio e halogênio
d) alcalino, halogênio e gás nobre
e) alcalino terroso, calcogênio e gás nobre
Resposta: Alternativa c) alcalino terroso, calcogênio e halogênio.
2. (UFU) No início do século XIX, com a descoberta e o isolamento de diversos elementos químicos, tornou-se necessário classificá-los racionalmente, para a realização de estudos sistemáticos. Muitas contribuições foram somadas até se chegar à atual classificação periódica dos elementos químicos. Em relação à classificação periódica atual, responda:
Como os elementos são listados, sequencialmente, na tabela periódica?
Resposta:
A tabela periódica classifica elementos químicos em sequências de ordem crescente de número atômico. Esse número corresponde à quantia de prótons no núcleo do átomo.
Essa metodologia de classificação foi proposta por Henry Moseley, que reconfigurou a tabela proposta por Dmitri Mendeleev. Um elemento pode ser encontrado na tabela pela família e período em que está inserido. Essa distribuição ocorre da seguinte forma:
- Grupos ou famílias (18 sequências verticais): grupos de elementos que apresentam características semelhantes.
- Períodos (7 sequências horizontais): número de camadas eletrônicas que o elemento apresenta.
3. (UEFS) Existe um conjunto de elementos químicos que apresenta como principais características: maus condutores de calor, opacos, não dúcteis e não maleáveis. Os elementos que apresentam essas características são denominados:
a) semimetais
b) gases nobres
c) não metais
d) elementos de transição simples
e) elementos de transição interna
Resposta: Alternativa c) não metais.
São chamados de não metais justamente por apresentarem características opostas às que definem um elemento como metal (condutor de calor, brilho, ductibilidade e maleabilidade)
4. (UDESC) Em 1869 Dmitri Mendeleev (1834-1907) apresentou à comunidade científica a lei periódica dos elementos. Sentindo-se seguro da validade de sua classificação, deixou posições vazias na tabela, para elementos que viriam a ser descobertos. Predisse, com uma precisão surpreendente, suas propriedades; para isso utilizou como base as propriedades dos elementos vizinhos, tendo fundamentado a atual classificação periódica dos elementos. Com base nas propriedades periódicas dos elementos, analise as informações abaixo.
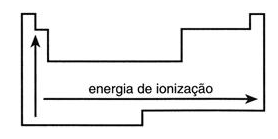
I – Os elementos do Bloco s apresentam baixa energia de ionização; seus elétrons são perdidos com facilidade.
II – As energias de ionização dos elementos do bloco p são menores do que as dos elementos do bloco s.
III – Todos os elementos do bloco d são metais, suas propriedades são intermediárias aos elementos do bloco s e p.
Assinale a alternativa correta.
a) Somente a afirmativa III é verdadeira.
b) Somente as afirmativas II e III são verdadeiras.
c) Somente as afirmativas I e III são verdadeiras.
d) Somente a afirmativa I é verdadeira.
e) Somente a afirmativa II é verdadeira.
Resposta: Alternativa: c) Somente as afirmativas I e III são verdadeiras.
A afirmativa II está incorreta pois a energia de ionização dos elementos do bloco p é maior do que a dos elementos do bloco s.
5. (UFPI) Assinale a alternativa em que o elemento químico cuja configuração eletrônica, na ordem crescente de energia, finda em 4s2 3d3:
a) grupo 3 e 2º período.
b) grupo 14 e 2º período.
c) grupo 14 e 5º período.
d) grupo 5 e 4º período.
e) grupo 15 e 3º período.
Resposta: Alternativa: d) grupo 5 e 4º período.
O elemento pertence ao grupo 5, pois a soma dos elétrons mais externos com os mais energéticos é igual a 5 (4s2 3d3) e ocupa o 4º período, pois tem quatro camadas eletrônicas (4s).
6. (PUC-SP) Resolva a questão com base na análise das afirmativas abaixo.
I – A tabela periódica moderna atual está disposta em ordem crescente de massa atômica.
II – Todos os elementos que possuem 1 elétron e 2 elétrons na camada de valência são, respectivamente, metais alcalinos e metais alcalino terrosos, desde que o número quântico principal dessa camada (n ≠ 1).
III – Em um mesmo período, os elementos apresentam o mesmo número de níveis (camadas).
IV – Em um mesmo grupo (família), os elementos apresentam o mesmo número de níveis (camadas).
Conclui-se que, com relação à tabela periódica atual dos elementos químicos, estão corretas:
a) I e IV (apenas).
b) I e II (apenas).
c) II e III (apenas).
d) II e IV (apenas).
e) III e IV (apenas).
Resposta: Alternativa c) II e III (apenas).
I – A tabela periódica moderna atual está disposta em ordem crescente de número atômico.
IV – Em um mesmo grupo (família), os elementos apresentam o mesmo número de elétrons na última camada.
–
Gás Nobre, espero que estes exercícios tenham ajudado você a treinar seu conhecimento em classificação dos Elementos na Tabela! E se você quiser um auxílio no seu processo de estudo, venha estudar com a gente e realize seu sonho de cursar uma faculdade!
Gás Nobre, espero que estes exercícios tenham ajudado você a treinar seu conhecimento em Química Orgânica! E se você quiser um auxílio no seu processo de estudo, venha estudar com a gente e realize seu sonho de cursar uma faculdade!
Gás Nobre! Você tem dificuldades para entender conteúdos de Ciências da Natureza? Não fique triste! Eu, professor Paulo Valim, quero te contar um segredinho que os melhores estudantes do Brasil já conhecem, com a minha plataforma Ciência em Ação, você vai conseguir aprender Química, Física e Biologia de forma rápida e efetiva e garantir a sua aprovação ainda em 2020.
Não importa se você tem dificuldades com as matérias ou se essa é a primeira vez que você vai estudar Química, Física ou Biologia. No Ciência em Ação, nossos cursos são completos e aprofundados. Eu e a minha equipe ensinamos todo o conteúdo do começo ao fim de forma didática.
Que foi? Você tem dúvidas de que o que eu estou falando é verdade? Então, saca só, Gás Nobre! Liberei o primeiro módulo completo da minha plataforma Ciência em Ação totalmente grátis pra você experimentar! Curtiu? Clique aqui e aproveite para conhecer a melhor plataforma de Ciências da Natureza da web!
Bora reagir e realizar os seus sonhos?
Me acompanhe nas redes sociais: curta a minha página no Facebook, siga o meu Instagram, se inscreva no canal do Youtube e entre no meu canal do Telegram.