Fala Gás Nobre, hoje vamos falar sobre a temperatura de fusão e ebulição, que são as temperaturas em que uma substância passa do estado físico sólido para o líquido e do líquido para o gasoso, respectivamente.
Entende-se por temperatura de fusão a temperatura na qual uma substância pura passa do estado sólido para o líquido, ou seja, se funde, sendo específica de cada substância a temperatura de fusão é também chamada de ponto de fusão e representada pela sigla PF.
O ponto de fusão é uma característica da substância e pode ser utilizada para sua identificação em uma amostra desconhecida, por exemplo.
Já a temperatura de ebulição é a temperatura em que uma substância passa do estado físico líquido para o gasoso, ou seja, se vaporiza, assim como a temperatura de fusão, a temperatura de ebulição também é uma característica específica de cada substância.
A temperatura de ebulição é também chamada de ponto de ebulição e representada pela sigla PE, e por ser uma característica específica, também é utilizada na identificação de compostos.
Tanto o ponto de fusão quanto o de ebulição são as temperaturas em que ocorrem a mudança de estado físico em uma dada pressão, por exemplo, os pontos de fusão e ebulição da água são, respectivamente, 0º e 100ºC, quando a pressão é de 1atm (nível do mar).
As temperaturas de fusão (PF) e ebulição (PE) variam de acordo com a pressão. O gás de cozinha a 1atm e na temperatura ambiente se encontra no estado gasoso, mas sob pressão dentro do botijão encontra-se no estado líquido, por exemplo.
Leia mais em: Mudanças de Estado Físico da Matéria
Temperatura ou Ponto de Fusão (PF)
A mudança de estado sólido para o líquido, processo chamado de fusão, acontece quando as moléculas recebem energia na forma de calor.
Esta energia é convertida nas moléculas na forma de energia cinética, ou seja, agitação, consequentemente, quanto maior a agitação das moléculas, maior sua temperatura.
Quando determinada temperatura é atingida, a temperatura de fusão, a agitação das moléculas é tal que se têm uma diminuição significativa das interações internas entre as moléculas, acarretando assim na mudança de estado físico.
Durante a fusão da substância a temperatura permanece constante, pois, toda a energia está sendo usada unicamente para a mudança de estado físico.

Leia mais em:
Por que o sal faz o gelo derreter?
Por que a água quente congela mais rápido que a água fria?
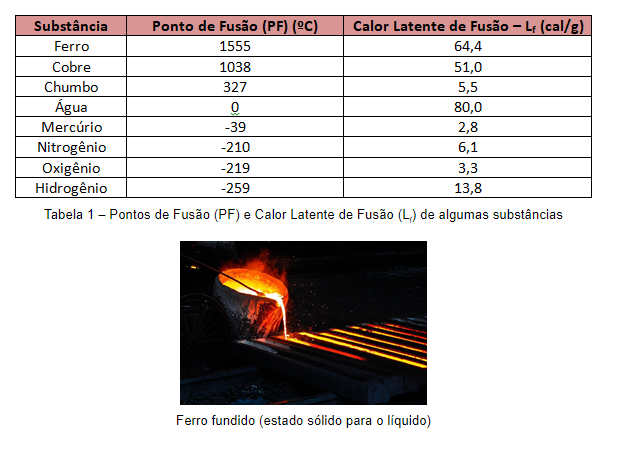
O calor necessário para mudar 1g da substância do estado sólido para o líquido é chamado de calor latente de fusão, sendo representado por Lf. Trata-se de uma propriedade característica de cada substância.
Temperatura ou Ponto de Ebulição (PE)
A ebulição é caracterizada pela rápida passagem do estado líquido para o gasoso (o processo lento é chamado de evaporação).
Da mesma forma que existe uma temperatura específica em que ocorre a mudança do estado sólido para o líquido, existe para a mudança do estado líquido para o gasoso.
Análogo ao processo de fusão, a ebulição ocorre quando uma substância recebe calor, este calor é convertido em energia cinética nas moléculas. E consequentemente ocorre a mudança de estado físico devido a diminuição da atração entre as moléculas e aumento de energia.
Durante todo o processo de ebulição, ou seja, de mudança de fases, a temperatura permanecerá constante. Toda a energia fornecida está sendo usada para a mudança de estado físico.
Já o calor necessário para mudar 1g de uma substância do estado líquido para o gasoso é chamado de calor latente de vaporização e é representado por Lv, também sendo específico para cada substância.

Alguns fatores influenciam o ponto de fusão (PF) e o ponto de ebulição (PE), como:
Pressão
Como citado anteriormente, o ponto de fusão e ebulição de uma substância são específicos para um determinado valor de pressão. Ou seja, variações no valor da pressão acarretam em variação da temperatura de fusão e ebulição de uma substância.
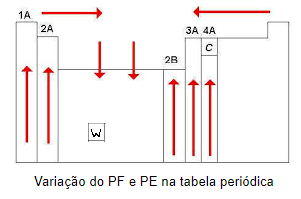
Posição na Tabela Periódica
Observa-se que os valores de temperatura de fusão e ebulição de substâncias simples, ou seja, formadas por um único elemento, possuem correlação com sua posição na tabela periódica, ou seja, se trata de uma propriedade periódica, como densidade ou raio atômico por exemplo.
Leia mais em: O que é a tabela periódica e como utilizá-la?
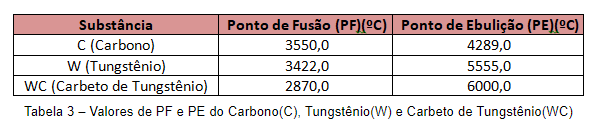
Entre os elementos químicos que apresentam as maiores temperaturas de fusão e ebulição encontram-se o tungstênio (W) e o carbono C. Devido a esta característica, o carbono é utilizado como eletrodo e o tungstênio como filamento de lâmpadas incandescentes.
Essa característica se reflete no Carbeto de Tungstênio (WC), material formado a partir destes 2 elementos e que possui aplicação industrial em máquinas e ferramentas devido a sua alta resistência térmica.
Leia mais em: Alotropia: O que você precisa saber?
Gás Nobre! Você tem dificuldades para entender conteúdos de Ciências da Natureza? Não fique triste! Eu, professor Paulo Valim, quero te contar um segredinho que os melhores estudantes do Brasil já conhecem, com a minha plataforma Ciência em Ação, você vai conseguir aprender Química, Física e Biologia de forma rápida e efetiva e garantir a sua aprovação ainda em 2020.
Não importa se você tem dificuldades com as matérias ou se essa é a primeira vez que você vai estudar Química, Física ou Biologia. No Ciência em Ação, nossos cursos são completos e aprofundados. Eu e a minha equipe ensinamos todo o conteúdo do começo ao fim de forma didática.
Que foi? Você tem dúvidas de que o que eu estou falando é verdade? Então, saca só, Gás Nobre! Liberei o primeiro módulo completo da minha plataforma Ciência em Ação totalmente grátis pra você experimentar! Curtiu? Clique aqui e aproveite para conhecer a melhor plataforma de Ciências da Natureza da web!
Bora reagir e realizar os seus sonhos?
Me acompanhe nas redes sociais: curta a minha página no Facebook, siga o meu Instagram, se inscreva no canal do Youtube e entre no meu canal do Telegram.