Todos os dias estamos em contato com diversos tipos de soluções, sejam bebidas, alimentos ou medicamentos, por isso, vamos falar hoje sobre algumas formas de determinar a concentração das soluções.
Existem várias formas de expressar a concentração de uma solução, vamos estudar algumas das principais, mas antes, vamos revisar rapidamente alguns conceitos de soluções. E aí, pronto para reagir?
Soluções
Soluções são misturas homogêneas constituídas por partículas de uma substância química dispersas (soluto) em outra substância química em maior quantidade (solvente).
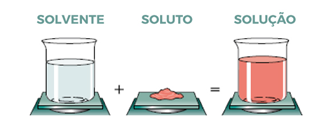
As soluções podem ser sólidas (ex: ligas metálicas), líquidas (ex: água do mar, álcool 70%) ou gasosas (ex: ar atmosférico).
Leia mais em:
Soluções: O que você precisa saber
Soluções: Coeficiente de Solubilidade (CS) e Classificação das Soluções
Concentração Comum (C) – (g/L)
Essa concentração é dada pela relação entre a massa do soluto (m1), expressa em gramas (g), e o volume da solução (V), expresso em litros.
É possível determinar a concentração comum através da fórmula:
Por exemplo, ao preparar 1 litro de suco, desses de pacote vendido em supermercados, você está preparando uma solução e sabendo a massa do pó do suco utilizado, você pode determinar a concentração comum do seu suco.
Vamos supor que o pacote do nosso suco possua 50g de suco em pó, teríamos uma concentração igual a:
C = m / V
C = 50g / 1L
C = 50g/L de suco.
Concentração em Quantidade de Matéria ou Concentração Molar (M) – (mol/L)
Essa concentração é dada pela relação entre a quantidade de matéria do soluto (n), expressa em número de mols, pelo volume da solução (V), expresso em litros.
Sabendo que o número de mols pode ser expresso pela equação abaixo:
n = m / MM
Onde,
n = número de mols (mol)
m = massa (g)
MM = massa molar (g/mol)
A concentração molar pode ser calculada pela equação:
M = n / V
ou
M = m / MM . V
Este é uma das formas de expressar a concentração de uma solução mais utilizada em laboratórios de química.
Porcentagem
Este tipo de concentração fornece uma relação entre o soluto e a solução através da porcentagem, ou seja, quantas unidades do soluto estão presentes em 100 unidades da solução (100%). Essa relação pode ser expressa através de relações de massa/volume (m/v), massa/massa (m/m) ou volume/volume (v/v).
As equações para determinar a porcentagem das soluções estão a seguir:
%(m/m) = msoluto / msolução
%(v/v) = Vsoluto / Vsolução
%(m/v) = msoluto / Vsolução
Por exemplo, o álcool vendido comercialmente tem sua concentração expressa em porcentagem do tipo volume/volume (v/v), no caso do álcool 70%, quer dizer que 70% do volume da solução trata-se de etanol (álcool etílico) e o restante da solução é água. O mesmo é observado para as demais porcentagens de álcool comercial (46 e 92,8%) ou para os teores de etanol em bebidas alcoólicas.
Partes por milhão (ppm) e Partes por bilhão (ppb)
A concentração por partes por milhão (ppm) e partes por bilhão segue a mesma ideia da concentração de soluções por porcentagem, no entanto, ao invés de determinar a quantidade de soluto presente em 100 unidades da solução, ppm determina a quantidade presente em 1 milhão de partes da solução e ppb em 1 bilhão de partes.
1 ppm = 1 unidade do soluto / 106 unidades da solução
1 ppb = 1 unidade do soluto / 109 unidades da solução
Para ter uma ideia da dimensão de 1 ppm e 1 ppb, vamos expressar em unidades de massa, por exemplo:
1 ppm = 1 mg de soluto / 106 mg de solução
1 ppm = 1 mg de soluto / kg de solução
1 ppb = 1 mg de soluto / 109 mg de solução
1 ppb = 1 mg de soluto / tonelada de solução
Mas se ppm e ppb representam soluções tão diluídas, ou seja, de concentrações muito pequenas, qual a sua aplicação?
Ppm e ppb são unidades de concentração muito utilizadas em perícias criminais e ambientais, onde existem elementos e substâncias químicas que em quantidades muito pequenas já apresentam risco para a saúde humana e de outras espécies, como toxinas, venenos e metais pesados (Chumbo (Pb), Mercúrio (Hg), Cádmio (Cd)).
Por exemplo, a cachaça, um tipo de bebida alcoólica, é preparada em alambiques de cobre e este metal, em excesso, causa danos à saúde humana e a legislação permite apenas a comercialização desta bebida que apresenta concentrações abaixo de 3ppm deste metal.

Gostou do assunto? Ficou interessado em saber como resolver exercícios envolvendo concentrações de soluções?
Leia mais em:
Cálculo de Concentração de Soluções
Cálculo de Concentração de Soluções: Exercícios Resolvidos
Gás Nobre! Você tem dificuldades para entender conteúdos de Ciências da Natureza? Não fique triste! Eu, professor Paulo Valim, quero te contar um segredinho que os melhores estudantes do Brasil já conhecem, com a minha plataforma Ciência em Ação, você vai conseguir aprender Química, Física e Biologia de forma rápida e efetiva e garantir a sua aprovação ainda em 2020.
Não importa se você tem dificuldades com as matérias ou se essa é a primeira vez que você vai estudar Química, Física ou Biologia. No Ciência em Ação, nossos cursos são completos e aprofundados. Eu e a minha equipe ensinamos todo o conteúdo do começo ao fim de forma didática.
Que foi? Você tem dúvidas de que o que eu estou falando é verdade? Então, saca só, Gás Nobre! Liberei o primeiro módulo completo da minha plataforma Ciência em Ação totalmente grátis pra você experimentar! Curtiu? Clique aqui e aproveite para conhecer a melhor plataforma de Ciências da Natureza da web!
Bora reagir e realizar os seus sonhos?
Me acompanhe nas redes sociais: curta a minha página no Facebook, siga o meu Instagram, se inscreva no canal do Youtube e entre no meu canal do Telegram.