O que é a tabela periódica e como utilizá-la? Essa é uma pergunta bastante comum entre as pessoas que nunca estudaram esse tema. A Ciência evolui com o passar do tempo. Novos conhecimentos, cada vez mais, são alcançados pela Humanidade, e um bom exemplo para ilustrar isso, é a forma como a organização dos elementos químicos se deu, ao longo do tempo, com a contribuição de diversos cientistas. Desde 1829, com o trabalho do químico alemão Johann Wolfgang Döbereiner (1780-1849), tivemos o estabelecimento de critérios para organizar os elementos, que após diversas contribuições, uma delas bastante famosa, feita em 1869 pelo químico russo Dmitri Ivanovitch Mendeleyev (1834-1907), chegamos na tão famosa e utilizada tabela periódica.
Nesse momento, não vamos percorrer o histórico de construção dessa ferramenta, mas sim, responder ao longo dessa postagem, algumas perguntas constantes, como:
- Para que serve a tabela periódica?
- Como interpretar a tabela periódica?
- O que são os números da tabela periódica?
- Porque é importante aprender a tabela periódica?
- Quantos são os elementos da tabela periódica?
E aí, preparado(a) para reagir?
A divisão da tabela periódica
A tabela periódica pode ser dividida através de 2 referenciais: períodos (horizontal) e grupos (vertical), onde cada “quadradinho” guarda as informações dos 118 elementos químicos conhecidos, representados através dos seus símbolos, oriundos da nomenclatura em latim.
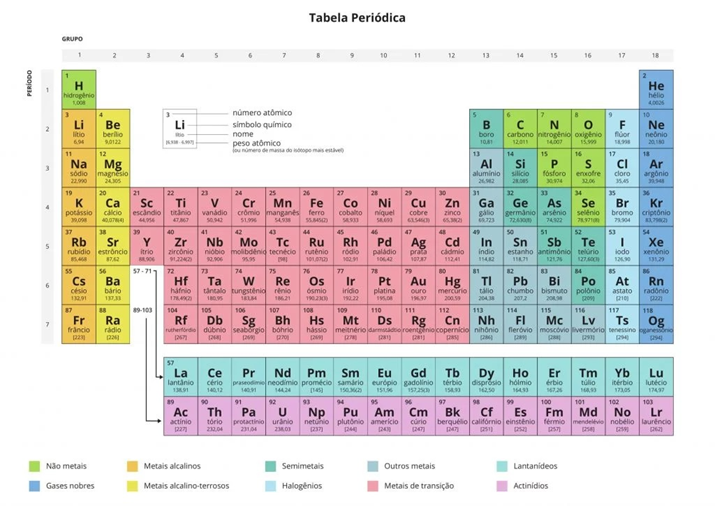
Observe que temos um total de 7 períodos (referencial na horizontal) e 18 grupos (referencial na vertical. Os elementos estão organizados em ordem crescente do número atômico. Através dessas informações, podemos descrever a posição de um elemento, como por exemplo, o Sódio: ele se localiza no terceiro período e no grupo 1, e apresenta número atômico 11.
Como extrair informações da tabela periódica?
O que é a tabela periódica e como utilizá-la? Para responder essa pergunta eu vou te ensinar a extrair as informações da tabela periódica.
Se por acaso você não sabe do que se trata a informação presente em cada “quadradinho” da tabela, saiba que sempre há uma legenda com as informações para você se guiar. Como essa, logo abaixo:
De acordo com a posição de um elemento, podemos extrair informações preciosas, como por exemplo, o número de elétrons no último nível de energia (camada de valência), ou até mesmo, o número de níveis de energia. Essa é uma das utilidades da tabela periódica.
Utilizando como exemplo o Cloro (número atômico 17), temos que o fato de este estar localizado no terceiro período, podemos dizer que ele apresentará também, três níveis de energia. Se fosse o elemento Chumbo (número atômico 82 e símbolo Pb), ele apresentaria 6 níveis de energia, pelo fato de estar localizado no 6° período. Ou seja, o período indica a quantidade de níveis de energia.
Os elétrons da camada de valência
Na ocasião de se achar os elétrons da camada de valência, podemos fazer a seguinte relação:
| Grupo 1= Família IA(metais alcalinos) | Grupo 2= Família IIA(metais alcalinoterrosos) | Grupo 13= Família IIIA(família do boro) | Grupo 14= Família IVA(família do carbono) |
| Grupo 15= Família VA(família do nitrogênio) | Grupo 16= Família VIA(família dos calcogênios) | Grupo 17= Família VIIA(família dos halogênios) | Grupo 18= Família VIIIA(família dos gases nobres) |
Esses elementos que estão nas famílias do tipo “A”, são chamados de elementos representativos, e os elementos localizados nos grupos 3 ao 12, são chamados de elementos de transição, e são representados por famílias do tipo “B”. Algumas tabelas trazem essa informação, como por exemplo, a tabela periódica do vestibular da UERJ:
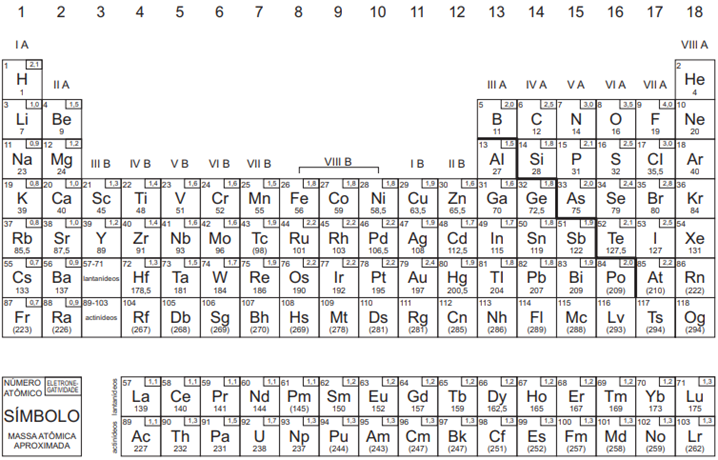
Voltando ao Cloro, o fato de estar localizado na família VIIA, podemos dizer que este apresenta 7 elétrons na última camada. O mesmo vale para os demais elementos localizados na mesma família: Flúor, Bromo, Iodo, Astato e Tenessino. No caso do Chumbo, pelo fato de estar na família IVA, ele apresenta 4 elétrons na última camada.
Vale ressaltar que essa dica vale para os elementos representativos. Os elementos de transição seguem um padrão que não vamos abordar nesse momento.
Em muitas situações, essa informação é relevante para que possamos, por exemplo, analisar o tipo de ligação química existente em um determinado composto.
Os elementos mais à esquerda da tabela são os metais, que possuem características determinantes, como por exemplo, baixa eletronegatividade, tendência de formar cátions, etc. Mais à direita, temos os não metais, que possuem características como alta eletronegatividade, tendência de formar ânions, etc.
Se por acaso precisamos ver o tipo de ligação química entre o sódio e o cloro, basta ver que o fato de serem metal e não metal, respectivamente, eu tenho a ligação do tipo iônica ocorrendo.
A tabela periódica é uma ferramenta importante para o estudo de química, onde é importante entender como se dá a sua organização e informações que se pode extrair. Muitas pessoas acham que é um “bicho de sete cabeças”, onde devemos decorar todas as informações. Esse tipo de pensamento não está correto, pois a tabela serve como um apoio presente nos estudos, avaliações e vestibulares, para que as pessoas possam compreender e extrair informações na resolução de problemas maiores. Por isso é importante aprender o que é a tabela periódica e como utilizá-la.
Quer estudar mais sobre a Tabela Períodica? Dá play nessa aula:
Leia a carta do prof. Paulo Valim sobre a pandemia do coronavírus: