A temática das ligações químicas é algo especial para os vestibulares tradicionais, provas militares, ENEM, ou até mesmo as provas escolares. É através das ligações químicas que podemos empregar vários conhecimentos que antecedem esse conteúdo, como por exemplo, a atomística e o estudo da tabela periódica, e não somente isso, é através das ligações químicas que construímos a base para compreender as diferentes propriedades existentes entre os compostos, ou seja, é um tema importantíssimo e você não deve vacilar!
Gás Nobre, nesse artigo vou lhe apresentar 3 questões de vestibulares sobre ligações químicas, e no final deste artigo, eu separei uma surpresa pra você \o/
Então, bora reagir?
Exercício 1: (FPS) Considere os átomos X, com número atômico 13, e os átomos Y com número atômico 8. Entre esses átomos forma-se um composto com a seguinte fórmula:
a) X3Y2 b) X2Y3 c) XY d) X4Y3 e) X2Y5
Exercício 2: (MACK) A fosfina é um gás auto-inflamável, formado por fósforo e hidrogênio, produzido na decomposição de matérias orgânicas. Assim, em cemitérios, por vezes, as pessoas se assustam ao se depararem com nuvens desse gás e, se correrem, devido ao deslocamento de ar, têm a impressão de que o fogo as acompanha. Esse fenômeno é conhecido por fogo-fátuo. Com relação à fosfina, é INCORRETO afirmar que:
Dado: número atômico P = 15, H = 1
a) tem fórmula molecular PH3.
b) possui três ligações covalentes sigma.
c) o fósforo possui um par de elétrons disponível.
d) não possui ligação pi.
e) tem fórmula estrutural P ≡ H.
Exercício 3: (CEFET MG) Para a realização de uma determinada atividade experimental, um estudante necessitou de um material que possuísse propriedades típicas de substâncias dúcteis, maleáveis, insolúveis em água e boas condutoras térmicas. Um material com essas propriedades resulta da ligação entre átomos de
a) Cu e Zn b) Na e Cl c) Fe e O d) F e Xe e) C e Si
Resposta da Questão 1:
[B]Consultando a tabela periódica, temos que X seria o alumínio (metal) e Y seria o oxigênio (ametal), o que configura uma ligação iônica.
A distribuição eletrônica de 13X: 1s2 2s2 2p6 3s2 3p1, e de 8Y: 1s2 2s2 2p4 , nos remete ao fato que X apresenta 3 elétrons na camada de valência, e Y apresenta 6 elétrons na camada de valência.
Nesse caso, temos que X possui tendência a formar cátion trivalente (3+), enquanto Y possui tendência a formar ânion bivalente (2-), e ao cruzar o valor dessas cargas em módulo, teremos X2Y3.
Resposta da Questão 2:
[E]Sendo a fosfina formada por fósforo (grupo 15, família VA) e hidrogênio (grupo 1, família IA), temos que a sua fórmula molecular seria PH3, pois o fósforo possui 5 elétrons na camada de valência (necessitando estabelecer 3 ligações covalentes para alcançar o octeto) e o hidrogênio possui 1 elétron na camada de valência (necessitando estabelecer 1 ligação covalente).
Com base nisso, temos que 3 hidrogênios são necessários para estabilizar 1 fósforo.
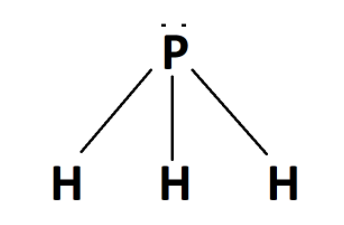
Como as ligações entre os átomos são do tipo simples, temos caracterizado a ligação do tipo sigma.
Resposta da Questão 3:
[A]De acordo com as propriedades mencionadas no enunciado, temos todas as descrições das propriedades estudadas nas ligações metálicas. Com base nisso, temos que a alternativa A contém um composto formado por 2 metais, o cobre e o zinco.
Surpresa \o/
Gás Nobre, você que parou aqui para estudar sobre as ligações químicas, que tal se aprofundar no tema, ver mais exercícios, e criar bases sólidas nesse tema?
Para isso, organizei uma super sequência de aulas completas do assunto, para você estudar no conforto da sua casa como se fosse em uma aula presencial comigo. Olha só que coisa boa, não é?
Então é só acessar o link abaixo, e reagir comigo 😀
Além disso, se você quiser ler mais artigos sobre esse tema, não deixe de acessar outros links que vão lhe ajudar:
Artigo 1: Ligações iônicas no nosso cotidiano
Artigo 2: Ligações metálicas no nosso cotidiano
Artigo 3: Ligações covalentes no nosso cotidiano
Artigo 4: Ligações covalentes no nosso cotidiano parte 2
Gás Nobre! Você tem dificuldades para entender conteúdos de Ciências da Natureza? Não fique triste! Eu, professor Paulo Valim, quero te contar um segredinho que os melhores estudantes do Brasil já conhecem, com a minha plataforma Ciência em Ação, você vai conseguir aprender Química, Física e Biologia de forma rápida e efetiva e garantir a sua aprovação ainda em 2020.
Não importa se você tem dificuldades com as matérias ou se essa é a primeira vez que você vai estudar Química, Física ou Biologia. No Ciência em Ação, nossos cursos são completos e aprofundados. Eu e a minha equipe ensinamos todo o conteúdo do começo ao fim de forma didática.
Que foi? Você tem dúvidas de que o que eu estou falando é verdade? Então, saca só, Gás Nobre! Liberei o primeiro módulo completo da minha plataforma Ciência em Ação totalmente grátis pra você experimentar! Curtiu? Clique aqui e aproveite para conhecer a melhor plataforma de Ciências da Natureza da web!
Bora reagir e realizar os seus sonhos?
Me acompanhe nas redes sociais: curta a minha página no Facebook, siga o meu Instagram, se inscreva no canal do Youtube e entre no meu canal do Telegram.