Fala Gás Nobre, hoje falaremos sobre as questões que mais comumente caem no ENEM sobre combustíveis. Será que você está preparado para responder as perguntas sobre esse assunto?
Esse é um tema que cai de alguma forma em praticamente todas as edições do ENEM. Isso se deve principalmente pela característica do ENEM em abordar questões voltadas à química ambiental e ao fato de que o uso de combustíveis fósseis ou alternativos está diretamente relacionado às questões ambientais.
Os dois conteúdos que mais caem no ENEM são Química Ambiental e Química Orgânica, respectivamente. E os combustíveis, tanto os fósseis (diesel, gasolina, carvão, querosene) quanto os renováveis (etanol, biodiesel, biomassa) são moléculas orgânicas cujo uso afeta diretamente positiva ou negativamente o meio ambiente. Ou seja, questões envolvendo-os são muito comuns por estarem relacionadas a estas duas áreas que comumente caem no ENEM.
Leia mais em: Quais são as vantagens do curso extensivo ENEM e medicina 2021
De forma geral, você deve estar atento a 3 principais aspectos:
I. Reações de combustão completa e incompleta;
II. Impacto ambiental do uso dos combustíveis fósseis;
III. Tipos de combustíveis: combustíveis fósseis e combustíveis renováveis.
Vamos falar brevemente de cada um destes aspectos e os conceitos que você deve treinar e dominar para ir bem em questões desse assunto.
I. Reações de combustão completa e incompleta
A obtenção de energia, seja ela elétrica, térmica ou mecânica, através de combustíveis fósseis se dá pela queima dos mesmos. Por isso, é muito importante você conhecer a fórmula química dos principais combustíveis e saber balancear corretamente a reação química de queima completa e incompleta destes compostos.
A queima destes compostos gera calor, luz e energia, podendo gerar eletricidade, aquecimento e movimento, dependendo da sua aplicação.
Aqui saliento as diferenças entre a queima completa e a incompleta destes compostos. Os principais combustíveis fósseis são o gás de cozinha (C4H10), gasolina (C8H18), etanol (CH3CH2OH) e o carvão (C) e a reação de queima se dá entre estes compostos e o gás oxigênio (O2). Como produtos teremos o gás carbônico (CO2) e a água (H2O) para a queima completa e o monóxido de carbono (CO) e/ou fuligem (C) na queima incompleta.
Leia mais em: A emissão de carbono pode ser maior do que se pensava
Desta forma, teremos algo assim:
Reação completa:
Combustível + O2 → CO2 + H2O
Reação incompleta:
Combustível + O2 → CO + H2O ou C + H2O
É super importante Gás Nobre, que você faça o balanceamento correto destas equações químicas.
Leia mais em:
Balanceamento por tentativas
Balanceamento por oxirredução
II. Impacto ambiental do uso dos combustíveis fósseis
Como citado anteriormente, a queima desses combustíveis libera CO2 na atmosfera, sendo este um dos principais gases do efeito estufa. Acredita-se que o uso intenso destes combustíveis tem agravado o efeito estufa no planeta e têm-se então uma preocupação mundial sobre o uso destes compostos.
Além disso, nestes combustíveis é comum a presença de impurezas, geralmente constituídas de compostos que contêm enxofre (S) e nitrogênio (N). Estes compostos, sob a forma de óxidos de enxofre e nitrogênio, quando lançados na atmosfera através da queima destes combustíveis podem formar a chamada chuva ácida, que é bastante abordada no ENEM e em diversos outros vestibulares.
Sobre questões sobre a chuva ácida e outras questões de química ambiental recomendo a leitura de um artigo que escrevi aqui no blog sobre Química Ambiental no ENEM.
III. Tipos de Combustíveis
1) Fósseis
O primeiro combustível largamente utilizado pelo homem foi a madeira e o carvão vegetal, sendo substituído pelo carvão mineral com a Revolução Industrial. Com a descoberta de métodos eficientes de exploração do petróleo, este, juntamente com o carvão mineral, passou a representar mais de 75% da matriz energética mundial.
O petróleo e o carvão derivam da decomposição de material animal e vegetal, diferindo-se entre si pelo tempo de formação, estado físico e profundidade. O carvão vem de fontes mais jovens e podem ser encontrados em minas próximas à superfície no estado sólido, enquanto o petróleo é um líquido viscoso e possui idades muito superiores à do carvão, sendo encontrado em camadas profundas do solo ou do fundo do mar.
Leia mais em: Os impactos do petróleo no meio ambiente
O petróleo, após extraído, é processado e passa por etapas de refinamento e craqueamento, onde suas várias frações de compostos que o constituem podem ser separadas. O processo de separação das frações de petróleo ocorre através de uma coluna de fracionamento e chama-se destilação fracionada. Dentre estas frações, a de maior destaque dentre os combustíveis está a gasolina. Gás de cozinha, diesel e querosene são outras que podem ser citadas.
Leia mais em:
Aula: Separação de Misturas
Separação de Misturas: Parte I
Separação de Misturas: Parte II
A queima destes combustíveis gera enormes quantidades de CO2 e suas fontes podem esgotar um dia, ou seja, nessa perspectiva entram em cena os combustíveis renováveis como uma alternativa ao uso dos fósseis.
2) Renováveis
Existem algumas fontes de energias ditas renováveis, que são: usinas hidrelétricas, solares, eólicas, geotérmicas e que se utilizam de biomassa como combustível.
Vamos focar no uso de biomassa e biocombustíveis. A biomassa é formada por restos de madeira, resíduos agroindustriais (bagaços, cascas, folhas, entre outros), plantas, alimentos, animais, algas, entre outros. O gás metano formado em lixões também pode ser utilizado como combustível. Ou seja, a biomassa é o reaproveitamento de material que seria descartado como fonte de energia.
Quanto aos biocombustíveis, os principais são o etanol e o biodiesel e aqui já deixo a dica para você ficar por dentro das reações de obtenção destes 2 compostos. O etanol é obtido através de um processo fermentativo, onde microrganismos convertem o açúcar da cana-de-açúcar em etanol e CO2. Já o biodiesel é obtido através de uma reação chamada de transesterificação.
Leia mais em: Biodiesel
Mas você pode estar se perguntando, se a energia é obtida através da queima, não vai liberar CO2 também?
Vai sim, no entanto, como esses combustíveis e essa biomassa provém de plantas a quantidade de CO2 é novamente assimilada pelas plantas que vão servir futuramente para produção de mais biocombustível. Ou seja, têm-se um ciclo auto sustentável de liberação e absorção de CO2, que não existe na queima de combustíveis fósseis. Isto é, o uso de combustíveis renováveis não afeta no ciclo biogeoquímico do carbono.
Leia mais em: Ciclos biogeoquímicos: Tudo o que você precisa saber
Gás Nobre, vou trazer aqui algumas questões envolvendo combustíveis que caíram nas últimas provas do ENEM para você ter uma ideia do que esperar que caia sobre esse assunto.
Já adianto que o ENEM tem a característica de contextualizar suas questões com um assunto em específico, mas de abordar e necessitar uma série de outros conceitos para que a pergunta seja respondida, então fique ligado e bora reagir.
ENEM (2012) – O benzeno é um hidrocarboneto aromático presente no petróleo, no carvão e em condensados de gás natural. Seus metabólitos são altamente tóxicos e se depositam na medula óssea e nos tecidos gordurosos. O limite de exposição pode causar anemia, câncer (leucemia) e distúrbios do comportamento. Em termos de reatividade química, quando um eletrófilo se liga ao benzeno, ocorre a formação de um intermediário, o carbocátion. Por fim, ocorre a adição ou substituição eletrofílica.
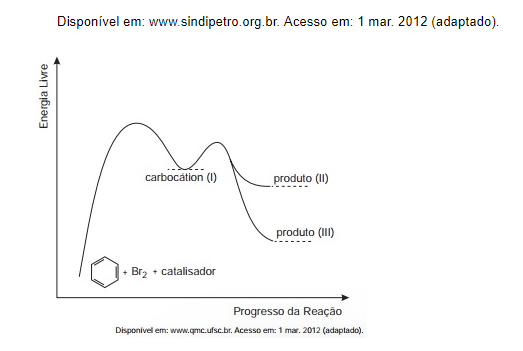
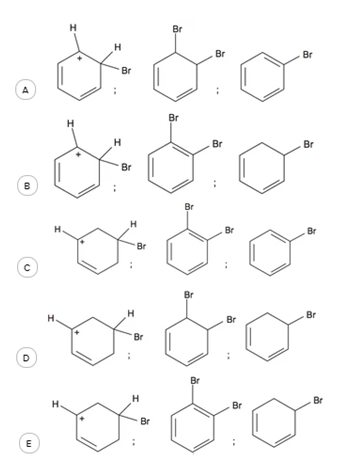
Com base no texto e no gráfico do progresso da reação apresentada, as estruturas químicas encontradas em I, II e III são, respectivamente:
Já começamos com uma reação envolvendo conhecimentos sobre Reações Químicas, que é um conteúdo de Química Orgânica bastante temido pelos alunos de forma geral. Aproveito para adiantar que as demais questões que selecionei aqui cobram de alguma forma conceitos de reações químicas, ou seja, é super importante que você dê uma atenção especial para esse assunto durante seus estudos.
Leia mais em: Reações com compostos orgânicos
Gás Nobre, o enunciado cita a formação de um intermediário com carbocátion, que é um carbono com uma carga positiva. O carbocátion só pode ser formado em um dos carbonos onde a ligação dupla do benzeno foi quebrado, ou seja, apenas a letra A ou a letra B podem estar corretas. A reação é completada com a adição de mais um bromo em um dos produtos (II) e saída de um hidrogênio no outro (III). Com a adição de mais um bromo, cada carbono estará ligado a 2 outros carbonos, 1 hidrogênio e 1 bromo, ou seja, não poderá estar fazendo uma dupla ligação como mostra o composto II da letra B, ou seja, apenas a letra A está correta. Por fim, o composto III temos a saída de um hidrogênio e a formação da dupla para que o composto siga a regra do octeto.
Gabarito: A
Para este tipo de questão sugiro estudar sobre reações de alcenos e regra do octeto.
Vamos para mais uma?
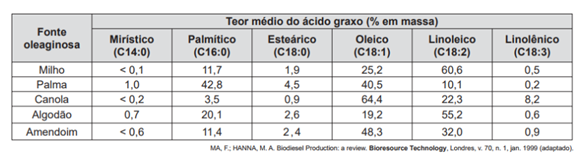
ENEM (2014) – O biodiesel não é classificado como uma substância pura, mas como uma mistura de ésteres derivados dos ácidos graxos presentes em sua matéria-prima. As propriedades do biodiesel variam com a composição do óleo vegetal ou gordura animal que lhe deu origem, por exemplo, o teor de ésteres saturados é responsável pela maior estabilidade do biodiesel frente à oxidação, o que resulta em aumento da vida útil do biocombustível. O quadro ilustra o teor médio de ácidos graxos de algumas fontes oleaginosas.
Qual das oleaginosas apresentadas produziria um biodiesel de maior resistência à oxidação?
a) Milho.
b) Palma.
c) Canola.
d) Algodão.
e) Amendoim.
Gás Nobre, aqui chamo atenção para a representação dos ácidos graxos, olhando o quadro temos, por exemplo, o Ácido Palmítico, representado pelo código C16:0, isso quer dizer que ele tem uma cadeia carbônica com 16 carbonos saturadas, ou seja, com ligações simples. Já o Ácido Linoleico é representado pelo código C18:2, que quer dizer que ele possui 18 carbonos na sua cadeia e possui 2 insaturações, ou seja, ligações duplas. Beleza Gás Nobre?
Leia mais em: Classificação das cadeias carbônicas
Desta forma, o enunciado da questão cita que o biodiesel produzido por óleos com maiores teores de ácidos graxos saturados apresentam maior resistência a oxidação e nos questiona qual das oleaginosas apresentadas produziria o biodiesel mais resistente. Ou seja, temos que identificar no quadro qual das oleaginosas possuí o maior teor dos ácidos Mirístico (C14:0), Palmítico (C16:0) e Esteárico (C18:0).
Logo, o biodiesel com maior resistência a oxidação seria o produzido a partir do óleo de Palma, que possui o maior percentual de ácidos graxos saturados em sua composição.
Gabarito: B
ENEM (2015) – Hidrocarbonetos podem ser obtidos em laboratório por descarboxilação oxidativa anódica, processo conhecido como eletrossíntese de Kolbe. Essa reação é utilizada na síntese de hidrocarbonetos diversos, a partir de óleos vegetais, os quais podem ser empregados como fontes alternativas de energia, em substituição aos hidrocarbonetos fósseis. O esquema ilustra simplificadamente esse processo.
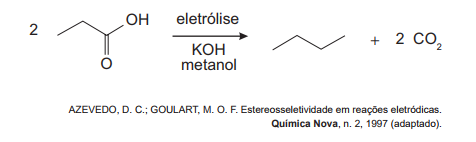
Com base nesse processo, o hidrocarboneto produzido na eletrólise do ácido 3,3-dimetil-butanoico é o:
a) 2,2,7,7-tetrametil-octano
b) 3,3,4,4-tetrametil-hexano
c) 2,2,5,5-tetrametil-hexano
d) 3,3,6,6-tetrametil-octano
e) 2,2,4,4-tetrametil-hexano
Olha só Gás Nobre, mais uma envolvendo Reações Químicas. Em questões assim é muito importante você estar dominando bem também a nomenclatura dos compostos orgânicos, pois as alternativas nos fornecem apenas a nomenclatura.
Observando a reação apresentada, vemos que temos a saída do grupo funcional (ácido carboxílico) da molécula e a junção da cadeia carbônica restante. Para descobrir o composto formado, precisamos saber quem é o reagente de partida e a molécula formada pela saída do grupo funcional.
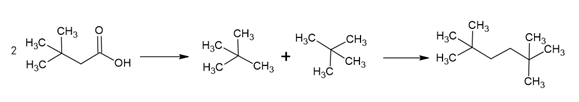
Com a saída do grupo funcional do ácido 3,3-dimetil-butanóico vamos ter a formação de 2 moléculas de 2,2-dimetil-propano, que ao reagir entre si, formaram um composto com 6 carbonos na cadeia principal (hexano) e 2 metils ligados ao carbono 2 e 2 ligados ao carbono 5. Logo, trata-se do 2,2,5,5-tetrametil-hexano, alternativa c.
Gabarito: C
Leia mais em: Principais compostos orgânicos
ENEM (2016) – O esquema representa, de maneira simplificada, o processo de produção de etanol utilizando milho como matéria-prima.
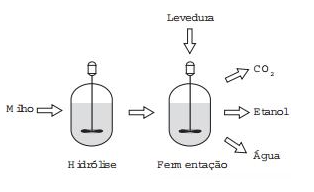
A etapa de hidrólise na produção de etanol a partir do milho é fundamental para que:
a) a glicose seja convertida em sacarose.
b) as enzimas dessa planta sejam ativadas.
c) a maceração favoreça a solubilização em água.
d) o amido seja transformado em substratos utilizáveis pela levedura.
e) os grãos com diferentes composições químicas sejam padronizados.
Aqui temos uma questão sobre a obtenção de biocombustíveis. Vou dar uma dica importante de bioquímica que ajudará a responder essa e outras questões que envolvam alimentação ou processos fermentativos. O amido e a celulose são polímeros formados por inúmeras moléculas de glicose e não são degradados ao menos que sua molécula seja quebrada em várias moléculas de glicose. Para que uma fermentação seja efetiva é importante que o amido seja quebrado em moléculas de glicose, que irão servir de substrato para as leveduras que a converterão em etanol, gás carbônico e água.
Leia mais em:
A química do pão
A ciência por trás da pizza
Em resumo, a hidrólise é uma etapa muito importante pois permitirá que o amido seja transformado em substrato para a levedura, aumentando a produção de etanol.
Gabarito: D
ENEM (2017) – O biodiesel é um biocombustível obtido a partir de fontes renováveis, que surgiu como alternativa ao uso do diesel de petróleo para motores de combustão interna. Ele pode ser obtido pela reação entre triglicerídeos, presentes em óleos vegetais e gordura animais, entre outros, e álcoois de baixa massa molar, como o metanol ou etanol, na presença de um catalisador, de acordo com a equação química:
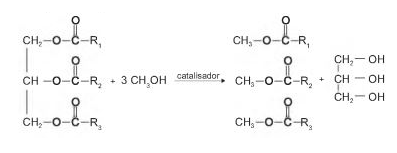
A função química presente no produto que representa o biodiesel é
a) éter.
b) éster.
c) álcool.
d) cetona.
e) ácido carboxílico.
Na sequência temos outra questão sobre obtenção de biocombustíveis e envolvendo novamente Reações Químicas. No entanto, o mais importante desta questão é estar atento às funções orgânicas. A reação de obtenção de biodiesel, como citado anteriormente, chama-se “transesterificação”, que é a conversão de um éster em outro éster. Logo, a função orgânica que está presente no biodiesel são os ésteres, representados pela parte em negrito:
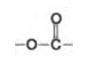
Gabarito: B
Leia mais em:
Reconhecimento das funções orgânicas
Funções Oxigenadas
Funções Nitrogenadas
ENEM (2010) – As cidades industrializadas produzem grandes proporções de gases como o CO2, o principal gás causador do efeito estufa. Isso ocorre por causa da quantidade de combustíveis fósseis queimados, principalmente no transporte, mas também em caldeiras industriais. Além disso, nessas cidades concentram-se as maiores áreas com solos asfaltados e concretados, o que aumenta a retenção de calor, formando o que se conhece por “ilhas de calor”. Tal fenômeno ocorre porque esses materiais absorvem o calor e o devolvem para o ar sob a forma de radiação térmica.
Em áreas urbanas, devido à atuação conjunta do efeito estufa e das “ilhas de calor”, espera-se que o consumo de energia elétrica
a) diminua devido à utilização de caldeiras por indústrias metalúrgicas.
b) aumente devido ao bloqueio da luz do sol pelos gases do efeito estufa.
c) diminua devido à não necessidade de aquecer a água utilizada em indústrias.
d) aumente devido à necessidade de maior refrigeração de indústrias e residências.
e) diminua devido à grande quantidade de radiação térmica reutilizada.
Gás Nobre, aqui, ainda que indiretamente, temos uma questão relacionada à liberação dos gases gerada pela queima dos combustíveis fósseis. Devido ao calor gerado pelo efeito estufa e pelas ‘ilhas de calor’ das cidades, a alternativa que melhor responde essa questão é a letra d, que cita o aumento consumo de energia para refrigeração de casas (ventiladores, ar condicionados) e de indústrias (sistemas de resfriamento e refrigeração, câmaras frias, entre outros).
Gabarito: D
ENEM (2009) – O etanol é considerado um biocombustível promissor, pois, sob o ponto de vista do balanço de carbono, possui uma taxa de emissão praticamente igual a zero. Entretanto, esse não é o único ciclo biogeoquímico associado à produção de etanol. O plantio da cana-de-açúcar, matéria-prima para a produção de etanol, envolve a adição de macronutrientes como enxofre, nitrogênio, fósforo e potássio, principais elementos envolvidos no crescimento de um vegetal.
Revista Química Nova na Escola. no 28, 2008.
O nitrogênio incorporado ao solo, como consequência da atividade descrita anteriormente, é transformado em nitrogênio ativo e afetará o meio ambiente, causando:
a) o acúmulo de sais insolúveis, desencadeando um processo de salinificação do solo.
b) a eliminação de microorganismos existentes no solo responsáveis pelo processo de desnitrificação.
c) a contaminação de rios e lagos devido à alta solubilidade de íons como NO3− e NH4+ em água.
d) a diminuição do pH do solo pela presença de NH3, que reage com a água, formando o NH4OH(aq).
e) a diminuição da oxigenação do solo, uma vez que o nitrogênio ativo forma espécies químicas do tipo NO2, NO− , N2O.
Gás Nobre, importante destacar que apesar de renováveis, os biocombustíveis não estão isentos de gerar danos ao meio ambiente. O CO2 gerado na sua queima é controlado pelo plantio das plantas que irão produzir mais deste combustível, no entanto, o uso de monoculturas e o uso excessivo de agrotóxicos e fertilizantes pode ocasionar danos e contaminações ao solo e corpos aquáticos.
O principal dano gerado pelo excesso de fertilizantes (compostos nitrogenados) que eu cito no texto sobre os ciclos biogeoquímicos, no caso do ciclo do nitrogênio, é a disponibilização de íons nitrogenados (nitrato, NO3– e amônio, NH4+) em corpos aquosos e a consequente eutrofização destes lugares.
Gabarito: C
Beleza Gás Nobre? Bastante coisa não? Mas fique tranquilo, seguindo as dicas que te passei você tem tudo pra ir super bem nas questões envolvendo esse assunto.
Leia mais em: A química no ENEM: 5 assuntos que você deve estudar
Reforço aqui que estar ninja em nomenclatura de compostos orgânicos, funções orgânicas e reações químicas, dominar esses assuntos vai ser um grande diferencial não apenas para questões envolvendo combustíveis, mas diversas outras de Química Orgânica e Química Ambiental. Bora revisar esses assuntos então. Reage!
Gás Nobre! Você tem dificuldades para entender conteúdos de Ciência da Natureza? Não fique triste! Eu, professor Paulo Valim, quero te contar um segredinho que os melhores estudantes do Brasil já conhecem, com a minha plataforma Ciência em Ação, você vai conseguir aprender Química, Física e Biologia de forma rápida e efetiva e garantir a sua aprovação ainda em 2020.
Não importa se você tem dificuldades com as matérias ou se essa é a primeira vez que você vai estudar Química, Física ou Biologia. No Ciência em Ação, nossos cursos são completos e aprofundados. Eu e a minha equipe ensinamos todo o conteúdo do começo ao fim de forma didática.
Que foi? Você tem dúvidas de que o que eu estou falando é verdade? Então, saca só, Gás Nobre! Liberei o primeiro módulo completo da minha plataforma Ciência em Ação totalmente grátis pra você experimentar! Curtiu? Clique aqui e aproveite para conhecer a melhor plataforma de Ciência da Natureza da web!
Bora reagir e realizar os seus sonhos?
Me acompanhe nas redes sociais: curta a minha página no Facebook, siga o meu Instagram, se inscreva no canal do Youtube e entre no meu canal do Telegram.